
随着纳米技术在食品工业全产业链的高速发展,从工程化添加、包装迁移到加工衍生的各类食源性纳米颗粒(FNPs)在膳食中的暴露水平逐渐提升,对其的安全性评价从传统单一的理化性质分析逐渐转向深层的细胞与分子生物学效应研究。本文介绍FNPs的多元化来源及理化性质,阐述其跨越肠道屏障的细胞吸收机制与影响因素(纳米颗粒尺寸、表面电荷及亲疏水性等),分析FNPs进入细胞后诱发的级联生物学效应(如线粒体损伤、氧化应激、细胞自噬、脂质代谢异常等)及相关的安全性研究进展。本文旨在阐明食源性纳米颗粒在功能高效与潜在毒性之间的结构-效应关联机制,分析全周期安全性风险,为全面理解纳米颗粒对人体的长效健康影响提供思路。最后,本文提出从单纯的“毒性评估”向“安全与功能性一体化设计”转型的研究展望,旨在精准调控FNPs在胃肠道内的稳定性及降解动力学,在规避对正常细胞非靶向性损伤的同时,保留其营养递送或辅助抗癌的高效功能,为构建食品纳米技术的全生命周期安全体系提供思路。
1 食源性纳米颗粒的分类与基本性质
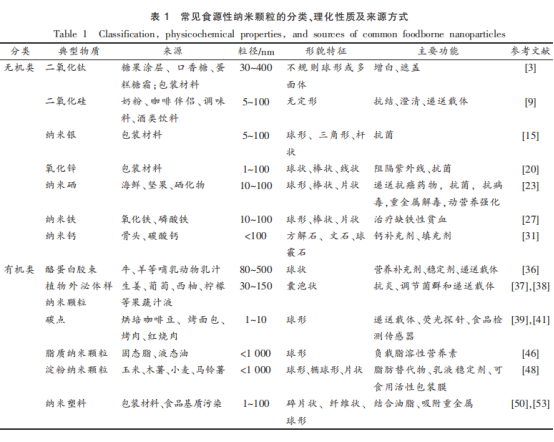
食源性纳米颗粒(FNPs)是指在食品生产、加工、贮藏和食用过程中存在于食品基质中纳米尺寸(1~1 000 nm)的物质。根据其化学结构分为无机纳米颗粒和有机纳米颗粒,两类颗粒在形貌特征、尺寸结构、成分构成以及来源机制均有显著差异。按照来源来划分,FNPs不仅包含为提升感官或营养性质而人工添加的工程纳米颗粒(ENPs),也包含天然存在于生物原料中的纳米颗粒以及食品加工过程中自组装形成的次生纳米颗粒。
常见食源性纳米颗粒的分类、理化性质及来源方式汇总见表1。
2 食源性纳米颗粒的细胞吸收
2.1 靶向细胞的类型及分布特征
食源性纳米颗粒经口摄入后,需突破由口腔酶、胃酸、肠道菌群及肠黏膜构成的多重生理屏障,其细胞摄取过程具有显著的部位特异性和细胞选择性,小肠上皮是纳米颗粒的核心摄取区域。肠上皮细胞是纳米颗粒经口摄入后的首要摄取载体,可通过多种主动转运机制实现内化。除小肠细胞以外,口腔上皮细胞则作为初始接触细胞,通过受体介导或非特异性吸附发生部分摄取。
突破肠屏障进入体循环后,FNPs同时通过全身循环扩散至多个器官的特定细胞类型中。肝脏细胞通过代谢转化与吞噬作用参与纳米颗粒清除,巨噬细胞利用模式识别受体在全身范围内高效摄取并转运纳米颗粒。值得关注的是,虽然受血脑屏障的严格限制,但是部分小粒径或靶向修饰的纳米颗粒仍可通过胞吞或跨细胞运输机制进入脑组织,与神经元及胶质细胞相互作用。金属纳米颗粒进入血液循环后,可能作用于血管壁的主要组分:内皮细胞和平滑肌细胞,影响血管功能并促进动脉粥样硬化发生。
2.2 纳米颗粒的细胞摄取途径
纳米颗粒进入细胞的摄取机制主要分为依赖囊泡形成的内吞作用以及不依赖囊泡的直接摄取途径,具体路径依赖于纳米颗粒的理化性质和靶细胞类型。
内吞作用是纳米颗粒进入细胞的主要途径,其核心机制为细胞膜发生内陷并包裹颗粒形成囊泡,可分为5种不同的途径,如图1所示。直接摄取途径不涉及囊泡的形成,而是纳米颗粒直接穿透或跨越细胞膜进入胞质,包括直接易位与膜融合2种方式(图2)。
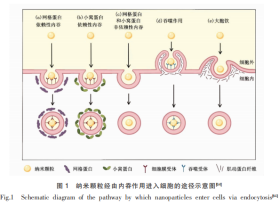
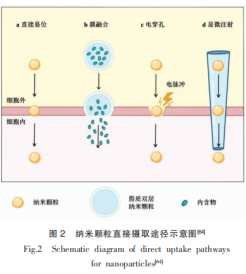
在特定研究或递送场景下,也可以采用物理手段辅助摄取,如利用电穿孔技术在膜上制造可控的瞬时孔道,或通过显微注射技术直接将颗粒注入胞质。
2.3 摄取过程的关键影响因素
细胞摄取NPs是一个由颗粒理化性质、细胞表型特征以及生理微环境共同调控的复杂过程。
颗粒理化性质起主导作用,其中尺寸是决定摄取路径与效率的首要因素,纳米颗粒的表面电荷也是调控细胞摄取的主要因素。此外,纳米颗粒形状对细胞摄取效率的影响尚未形成共识。机械刚度显著影响细胞吸收效率。若纳米颗粒表面修饰有特异性配体,如叶酸、转铁蛋白等,则可激活特定的受体介导途径,大幅提升靶向摄取效率。
纳米颗粒的摄取行为表现出显著的细胞特异性,由于具有失调的代谢活动和高流动性的膜结构,癌细胞及特定永生化细胞系通常较正常体细胞表现出更强的非特异性内吞能力。以巨噬细胞为代表的免疫细胞则通过表面特定的模式识别受体,高效识别并快速清除大粒径异物。
对于经口摄入的食源性纳米颗粒,胃肠道环境构成关键的外部变量,消化道内剧烈的pH值梯度波动与酶系降解作用可直接改变颗粒的原始表面性质。当纳米颗粒暴露于富含蛋白质的肠液、血浆等体液时,其表面会迅速吸附形成1层动态的“蛋白冠”,掩盖原有的表面化学特征,从而重塑其与细胞膜受体的相互作用模式。
3 食源性纳米颗粒引起的细胞生物学效应
3.1 氧化应激
氧化应激是纳米颗粒诱导细胞损伤的最普遍、核心的机制,其本质是纳米颗粒诱导细胞内活性氧(ROS)的产生速率高于细胞抗氧化系统的清除速率。纳米颗粒诱发ROS生成的机制是多维度的,包括非生物性的表面化学反应和生物性的细胞器功能障碍。
3.2 细胞自噬
自噬是细胞高度保守的自我降解过程,通过溶酶体清除受损的细胞器、错误折叠的蛋白质和外来病原体。纳米颗粒与细胞自噬的关系具有两重性,既能诱导自噬作为防御,也能阻断自噬导致毒性。
3.3 溶酶体胞吐与膜通透化
溶酶体不仅是降解中心,也是细胞内重要的Ca2+储存库,纳米颗粒在溶酶体内的积聚会触发Ca2+的释放,主要通过溶酶体胞吐和膜通透化两条路径,其内在机制与细胞命运密切相关。
3.4 线粒体损伤与功能障碍
线粒体是细胞的能量中心和ROS产生的主要场所,也是纳米颗粒细胞毒性的主要靶点。线粒体功能障碍是指线粒体无法维持正常的膜电位,ATP合成效率下降以及ROS过度产生的状态。
3.5 DNA损伤与基因毒性
部分具有尖锐边缘或小尺寸的纳米颗粒可能穿透核膜,与DNA直接相互作用,造成链断裂,同时可催化产生ROS,直接引起DNA碱基氧化或单/双链断裂。纳米颗粒诱发的慢性氧化应激是间接造成DNA持续损伤的主要驱动力,其引发的炎症反应可激活巨噬细胞等释放活性氮(RNS)与炎性因子,进一步加剧DNA损伤。某些纳米颗粒还可能干扰DNA复制与修复相关的酶系统,抑制细胞自身的修复能力。纳米颗粒还能在不改变DNA序列的情况下影响基因表达。
3.6 脂滴累积与脂质代谢
纳米颗粒进入细胞后,往往会引起脂质代谢的显著改变,表现为脂滴的异常累积或清除。
3.7 pH值稳态失衡
具有阳离子表面电荷的纳米颗粒进入溶酶体,大量结合质子,氯离子随之内流,导致溶酶体渗透压急剧升高,水分子涌入,最终引起溶酶体肿胀甚至破裂。此过程释放了纳米颗粒、各类水解酶和高浓度的质子到中性细胞质中,引起细胞质酸化坏死,干扰细胞骨架蛋白的组装和代谢酶活性。
4 食源性纳米颗粒的安全性研究进展
4.1 无机与有机食源性纳米颗粒的毒性机制
无机纳米颗粒因独特的物理、化学性质(如小尺寸效应、高比表面积、量子效应)而被广泛应用于食品添加剂和包装材料中,这些特性也赋予它们穿越生物屏障并诱发细胞应激的能力。研究表明,无机F-NPs的毒性机制主要集中在氧化应激,溶解产生的离子毒性以及对细胞器功能的干扰。
有机纳米颗粒通常由生物可降解材料构成,被认为具有更好的生物相容性,其安全隐患往往源于表面电荷密度、表面活性剂的选择以及载体本身的物理化学效应,风险更突出表现为通过肠道屏障穿透、免疫系统异常激活及肠道菌群紊乱构成的级联效应,引发慢性炎症与代谢紊乱等系统毒性。
综上所述,无机颗粒倾向于通过物理、化学途径直接损伤细胞结构,而有机颗粒更多表现为对生物屏障的渗透及微生态环境的干扰,表2列出两者毒性机制的差异性。
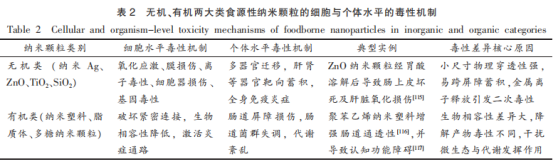
4.2 食源性纳米颗粒的安全性研究
4.2.1 微纳米塑料
食源性微纳米塑料(MNPs)主要来源为食品包装材料的迁移与环境污染物通过食物链的富集,广泛存在于海鲜、饮用水、食盐和塑料包装食品中,由于非有意添加且尺寸微小、成分复杂等特点,MNPs在检测方法统一、监管标准制定以及安全风险评估等方面均面临显著挑战。
NPs会诱导肠屏障损伤。同时NPs还会引发菌群失调,显著降低有益菌的丰度,破坏肠道微生态平衡。NPs不仅自身具有毒性,还可作为载体,吸附环境中的重金属、抗生素或持久性有机污染物,将其带入细胞内部,产生协同毒性。NPs的高穿透性使其能跨越人体最严密的生理屏障,如血睾屏障、血脑屏障等。NPs的生理毒性与其种类也有关联。
4.2.2 体外加工生成的纳米颗粒
食源性碳点(CDs)是一类尺寸通常小于10 nm的零维碳基荧光纳米材料,主要通过2种途径产生。在食品热加工(煎炸、烘烤、杀菌、酿造)过程中,食品中的还原糖与氨基酸发生美拉德反应或焦糖化反应,自组装形成碳点;或者以食品废弃物(玉米秸秆、果皮、咖啡渣)为前体,通过水热法、微波辅助法等“绿色化学方法”合成,常用于食品包装或检测。CDs凭借其天然的生物属性,内源性的抗菌抗氧化功能,独特的光学特性与热稳定性,在低浓度下通常表现出良好的生物相容性,为食品活性包装和安全检测提供了良好材料。然而,天然属性并不等同于绝对安全,高浓度或长期暴露可能导致生物蓄积、免疫反应与代谢紊乱。
4.2.3 体内消化衍生的纳米颗粒
体内衍生的纳米颗粒并非人为添加,而是食品基质(淀粉、蛋白质、脂质等)在口腔、胃、肠道的机械剪切和酶解消化过程中,通过自组装、重结晶或差异化降解形成的纳米级结构。
天然淀粉颗粒在原始状态下通常呈微米级尺寸,而在口腔至胃部的消化过程中,其结构中的无定形区会优先受到胃酸与水解酶的侵蚀。虽然抗性淀粉通常被认为具有小肠消化抵抗性,但是有研究表明,源自青香蕉、大米及莲子等基质的淀粉颗粒在机械剪切力与酶解环境的双重驱动下,其原始晶体结构发生改变,进而在胃肠道微环境中重排结构并自组装形成淀粉纳米颗粒。
5 结论
随着纳米技术在食品领域的深入应用,食源性纳米颗粒(FNPs)已成为日常膳食中不可忽略的组成部分。本文从不同来源出发,系统梳理天然存在、加工衍生及工程化添加的FNPs的理化特性,重点探讨其跨越肠道屏障的细胞吸收机制及后续的胞内生物学响应。基于现有研究,得出以下结论:
1)细胞吸收途径显著影响FNPs的胞内分布与生物学效应强度。FNPs并非仅依赖被动扩散进入细胞,其尺寸、表面电荷、亲疏水性等理化性质在很大程度上决定其摄取机制,如网格蛋白介导的内吞作用或直接膜融合。这些差异化的摄取方式一方面影响颗粒在细胞内的去向,部分颗粒滞留于溶酶体并被降解或外排,另一部分则可能逃逸至细胞质,诱发线粒体功能异常、氧化应激或脂质代谢紊乱。因此,深入揭示“理化性质-摄取途径-生物效应”之间的关联,是评估和调控FNPs安全性的关键依据。
2)关注衍生型纳米颗粒带来的潜在风险。当前安全性研究多聚焦于人工添加的无机纳米颗粒(如TiO2、Ag)或食品包装迁移的纳米塑料(如PP、PE),而对食品加工过程中自发形成的有机纳米颗粒(如碳点)以及在胃肠道消化环境中动态生成的纳米结构(如淀粉纳米颗粒)关注不足。这些在食品体系内原位生成或消化衍生的FNPs有一定的隐蔽性,往往不在常规安全监测范围,由其可能引起肠道菌群失衡和免疫炎症等长期慢性健康问题,值得研究人员高度警惕并深入研究。
3)推动从单纯的“毒性分析”向“安全与功能一体化设计”的研究范式转变。未来的研究方向不应局限于规避FNPs的潜在风险,更应辩证利用其生物活性。一方面,不仅需要揭示FNPs的毒性表现,也需要探索如何通过表面修饰、基质包埋等策略调控其在消化过程中的稳定性和降解行为,在保留其营养递送等功能的同时,降低其对正常细胞的细胞膜、线粒体、遗传物质等关键靶点的非必要接触与损伤。另一方面,挖掘部分对肿瘤细胞有特异性毒性的纳米颗粒,在保护自身组织安全的同时,发挥其潜在的辅助抗肿瘤功效,使FNPs在功能性与安全性之间达到平衡。
综上所述,对食源性纳米颗粒的安全性评价需立足于全生命周期视角:从生产加工、包装迁移到体内消化吸收的全过程。建立更接近人体真实消化环境的标准化评估模型,并在长期低剂量暴露背景下深入解析FNPs的构效关系,将成为未来制定食品纳米技术安全标准,推动功能性食品创新发展的重要路径。
原文链接:https://kns.cnki.net/kcms2/article/abstract?v=m07J8nP_wCENyWuYfdnml5SCGfqNA79C0R4JtXFVc12151M2RuTWp9NdWRqnSQ0X6RSdig7Q9HrCWQdSsm2ctvLJyMn1ANAfDSMcjlW9fPShnu05PBjaTaGS5yezC17ajZuiRjxodfqWbrTyYPzNmJJHpbs3DZBWpnt9VZJDTlyJOsoNml1ZVg==&uniplatform=NZKPT&language=CHS


