
在“大食物观”与可持续发展战略指引下,食用昆虫凭借卓越的营养效能与低碳足迹,成为缓解全球蛋白质供给危机的关键新质资源。然而,昆虫蛋白作为一种新型致敏原,其引发的食物过敏,尤其是与甲壳类和尘螨产生交叉反应的风险,已成为制约其产业化应用的主要瓶颈。研究表明,原肌球蛋白、精氨酸激酶等高度保守的泛过敏原是导致昆虫蛋白过敏的关键。然而,传统的单一评估模式难以精准区分原发与交叉致敏,且常规热加工技术面临过敏原热稳定性强、表位难以破坏等挑战。本文综述昆虫主要过敏原的分子特征与免疫机制,剖析现有风险评估体系的局限性,并构建整合临床病例分层、人工智能预测与体内外生物学验证的“精准识别-智能评估-靶向消减”的评价体系;同时,重点探讨酶解、发酵及高压、超声等新兴加工技术对致敏性消减的作用机理,并展望合成生物学与生物3D打印在源头低敏化中的应用潜力,旨在为建立科学的昆虫蛋白监管准则与构建产业免疫安全屏障提供理论支撑与决策参考。
1 食用昆虫及其致敏蛋白特性与致敏机制
1.1 食用昆虫资源利用现状
文献记录的可食用昆虫超过2100种,主要分属鞘翅目(约32%)、鳞翅目(约15.2%)、膜翅目(约15.5%)、直翅目(约14.1%)及半翅目(约11.4%)等。在食品及相关领域,国内外具有代表性和开发潜力的昆虫种类范围广泛,其分类、应用形式及开发阶段概况如表1所示。
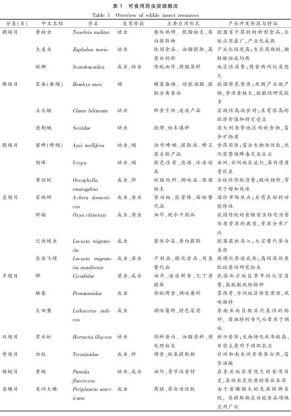
目前,产业化重点已集中到少数生物学特征明确、养殖技术成熟的物种。黄粉虫凭借极短的生长周期和高效的饲料转化能力,已成为研究最深入、应用最广泛的昆虫蛋白来源,是当前及未来市场的主要产品。家蚕蛹作为丝绸产业副产物,资源丰富且富含蛋白与油脂,在我国具有药食两用传统,在功能食品开发中展现出显著优势。直翅目昆虫如家蟋蟀与迁徙蝗虫,在亚洲具有稳定的消费基础,正逐步从街头小吃转向精深加工的蛋白配料。黑水虻目前主要用作饲料蛋白,然而其强大的生物转化能力正推动其向食品领域拓展,也为安全性评价带来新的挑战。
随着欧盟将黄粉虫、迁徙蝗虫等纳入“新型食品”监管框架,全球昆虫产业正步入合规化发展新阶段。人口增长与饮食结构转型使亚太地区有望成为全球最大的昆虫消费市场。然而,随着应用场景的拓展,相关暴露风险也随之上升。昆虫蛋白越来越多作为隐形配料(如蛋白粉、添加剂)进入食品体系,其作为新型过敏原对易感人群的威胁日益凸显。在此背景下,系统了解昆虫过敏原并建立科学的风险评估模型,已成为产业规范化发展的必要条件。
1.2 昆虫主要过敏原的分子鉴定与特征
昆虫蛋白的过敏原可大致分为3类,即:以原肌球蛋白为代表的肌原纤维结构蛋白,以精氨酸激酶为代表的细胞代谢酶类,以及血蓝蛋白等输运与存储蛋白。
1.2.1 原肌球蛋白
昆虫蛋白中的原肌球蛋白(TM)是肌肉组织的主要成分,也是介导昆虫、甲壳类与尘螨之间交叉反应的典型泛过敏原。TM在进化上高度保守,不同节肢动物之间序列相似性高,尤其在若干线性表位区域。TM具有较高的热稳定性与消化耐受性,这与其紧密的螺旋结构有关。常规烹饪(如煮沸、烘焙)虽可改变其二级结构,但往往无法完全破坏IgE结合的核心构象。然而,热与酶耐受性仍依赖于处理温度与时间、pH值及食品基质,个别条件下TM仍可部分降解。
1.2.2 精氨酸激酶
精氨酸激酶(AK)是一种广泛分布于无脊椎动物体内的单体磷酸激酶,在细胞能量稳态维持中起到ATP缓冲功能。
AK属于典型的球状功能蛋白,其三维结构由紧密折叠的α-螺旋与β-折叠构成,且不含二硫键。这一特点使其致敏性高度依赖天然构象,IgE识别表位多为构象型,对外界环境应力非常敏感,AK可被用作评估热加工对昆虫蛋白致敏性消减效果的指示蛋白。
近年来提出的“基质保护与免疫复性”假说认为,同一种蛋白,在不同食物基质与加工背景下,其免疫学命运(耐受或致敏)可能完全不同。在复杂食品基质中,变性的AK可能通过聚集或借助分子伴侣部分恢复结构,从而在热处理后仍保留一定免疫活性。此外,AK在蟑螂、尘螨及甲壳类动物中序列高度保守,也被视为介导“泛节肢动物综合征”的另一重要交叉反应原。对部分人群而言,AK甚至可作为原发性致敏原,在无海鲜过敏史的情况下引发独立的昆虫过敏反应。
1.2.3 其它昆虫过敏原
1.2.3.1 几丁质酶
几丁质酶属于糖基水解酶GH18家族,是昆虫蜕皮及外骨骼重塑的关键酶。在过敏领域,植物几丁质酶是“乳胶-水果综合征”的核心交叉反应原,能够在乳胶与多种植物性食物(如鳄梨、香蕉、栗子)之间介导显著的IgE交叉反应,其在乳胶-水果交叉致敏中的作用,主要源于该类酶N端保守的类橡胶蛋白结构域,该区域与主要乳胶过敏原共享IgE结合表位。昆虫几丁质酶主要定位于外骨骼,与其底物几丁质在空间上共存。值得注意的是,几丁质本身具有免疫刺激活性,可激活上皮细胞并诱导IL-33等警报素释放,从而启动并放大Th2型免疫应答。这种协同作用能够绕过经典抗原识别途径,并在相对低剂量暴露水平下诱发显著的Th2型炎症反应及气道高反应性。
1.2.3.2 血蓝蛋白
血蓝蛋白是节肢动物特有的含铜呼吸蛋白,常以六聚体或巨大多聚体形式存在,单亚基分子质量约70~80 ku,具有强免疫原性。值得注意的是,血蓝蛋白广泛游离于昆虫血淋巴中,在养殖加工环境中易随粉尘形成气溶胶,这种“吸入-食入”双重暴露路径使其成为诱发职业性哮喘的关键致敏原。
1.2.3.3 丝蛋白
丝蛋白包括丝素蛋白和丝胶蛋白,主要存在于家蚕等鳞翅目昆虫的丝茧中,具有高度的物种特异性、热稳定性及机械强度。这两类蛋白共同构成蚕茧的主要骨架,具有高度的物种特异性序列和组织表达特点,在结构和功能上与TM和AK的保守性不同。部分蚕蛹过敏患者仅对丝蛋白产生特异性IgE反应,而对TM、AK等泛过敏原无反应,且能耐受甲壳类食品。这表明丝蛋白是诱发原发性昆虫过敏的重要因子,可用于区分原发性致敏与交叉致敏。
1.2.3.4 肌球蛋白轻链
肌球蛋白轻链(MLC)是一类分子质量约18~22 ku的肌肉相关蛋白,广泛存在于节肢动物横纹肌中。虽然MLC本身致敏频率不高,但是在多过敏原共暴露时,它能通过多表位识别协同增强FcεRI交联效率,从而放大脱颗粒反应。这一机制有助于解释为何尘螨或蟑螂致敏者在首次或低剂量摄入甲壳类时即可出现明显症状,也提示蟑螂MLC可能并非单纯的伴随抗原。
1.3 昆虫蛋白原发过敏与交叉过敏的免疫机制
当具有消化抗性的昆虫过敏原片段成功通过肠道屏障后,便会诱发典型的IgE介导的I型超敏反应。这一过程涉及跨上皮转运、抗原呈递、Th2型免疫极化及效应细胞脱颗粒等复杂的过程,详见图1。
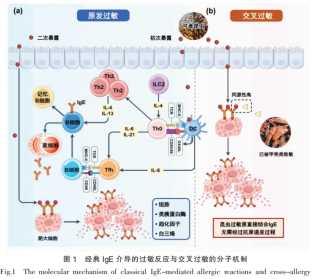
2 昆虫蛋白的致敏性评估框架体系
要将昆虫蛋白安全纳入人类膳食体系,必须建立科学、严谨的致敏性评估框架。鉴于昆虫蛋白与甲壳类、尘螨过敏原存在高度同源性,传统的单一评估方法已显不足。为此,本文构建一个从“临床风险分层”到“人工智能预测”,再经“生物学实验验证”,最终完成“综合风险判定”的闭环评估体系(图2),以系统量化并管理其致敏风险。
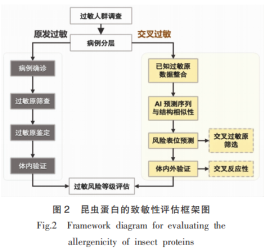
3 昆虫蛋白致敏性消减与控制策略
3.1 传统加工技术
3.1.1 热处理
热处理是降低昆虫蛋白致敏性的常见手段,其效果因昆虫种类、目标蛋白及加工条件而异,部分过敏原对热加工具有高度稳定性。
3.1.2 酶解与交联
酶解是通过特异性断裂蛋白质肽键来降低其致敏性的重要生物加工方法,其效果取决于水解程度。不同过敏原对酶的敏感性存在差异。酶解还可与交联技术或其它加工技术联用,通过改变蛋白聚集状态、构象与消化稳定性,进一步降低其致敏性。虽然酶解在降低IgE结合能力方面具有潜力,但是其应用仍面临挑战。一方面,现有证据多基于体外试验,需更多体内及临床验证;另一方面,酶解尤其是碱性蛋白酶水解,易产生苦味和特殊风味,可能影响产品接受度。目前,针对加工技术如何影响可食用昆虫感官品质的研究仍较缺乏,这是未来实现其商品化必须兼顾的方向。
3.1.3 美拉德反应
美拉德反应能通过共价修饰与构象变化显著影响蛋白质的致敏性。尽管相关机制研究多集中于甲壳类过敏原TM和AK,其结论对理解与调控昆虫蛋白致敏性仍具有参考价值。然而,美拉德反应的影响具有条件依赖性。在反应早期,使用葡萄糖、核糖等小分子糖可能因生成新表位而增强致敏性,麦芽三糖则未见类似效应。这一复杂性在昆虫蛋白中同样存在,例如糖基化可能增加黄粉虫蛋白的致敏性,且该效应严格依赖于反应条件。加工方式也是重要变量。例如,干燥条件可显著改变昆虫蛋白的微环境与理化状态。此外,超声等预处理能改变蛋白构象,暴露新的糖基化位点,增强反应效率,从而可能掩蔽IgE/IgG表位,最终降低抗体结合能力。
3.2 新兴技术
3.2.1 高压处理
高压处理(HPP)技术常用于微生物和酶的灭活,近年来已广泛应用于食品加工领域,其可通过诱导蛋白质变性和结构改变来降低其致敏性。此外,HPP还能与其它技术协同增强效果。例如,HPP辅助蛋白酶水解可显著提高黄粉虫蛋白的水解度和体外消化率,从而降低其免疫反应性。
3.2.2 微波/超声处理
微波处理能够引起蛋白质二级结构重排,如β-折叠增加、β-转角减少,从而破坏构象表位,降低IgE结合能力。
高强度超声处理也表现出降敏潜力。延长超声处理时间至20 min,可使TM含量降低约76%,并促使蛋白质断裂为小分子肽段,同时改变α‑螺旋与β‑折叠比例,提高体外消化性,显著降低IgE结合能力。超声处理对不同过敏蛋白的作用效果与处理条件密切相关。
联合应用微波或超声与其它技术可增强降敏效果。该联合方式在破坏蛋白质结构、促进活性肽生成的同时,显著削弱了TM的免疫反应性,说明其兼具功能改性与潜在减敏作用。超声-微波联合处理则可促使蛋白展开,疏水基团暴露,并改善凝胶网络结构。然而,此类结构重构对致敏表位稳定性及免疫反应性的具体影响,仍缺乏系统性的试验验证。
3.2.3 电场相关技术
脉冲紫外线(PUV)作为一种非热/低热加工方式,可在多种食品体系中通过紫外光激发改变蛋白质构象,进而显著降低IgE结合能力与免疫反应性。
脉冲电场(PEF)主要通过电穿孔效应影响蛋白质结构。虽然该技术在直接调控过敏原方面的研究尚处起步阶段,但是其诱导蛋白质结构变化的机制为探索其在昆虫致敏性管理中的应用提供了依据。
目前相关研究,特别是针对昆虫蛋白的探索,仍处于初步阶段。现有工作多集中于理化性质与体外结构表征,缺乏对关键致敏表位稳定性及体内免疫反应的系统评价。未来需要在标准化加工条件下,结合结构分析与免疫学方法,深入阐明其作用机制,并系统评估这些技术在降低食用昆虫过敏风险方面的有效性、安全性及应用可行性。
3.2.4 发酵
发酵能在较好地保留食品营养与感官品质的同时降低致敏性,也被视为一种兼具安全性与功能性的潜在降敏策略。在贝类与鱼类等传统过敏原的研究中,发酵已被证实可有效降解致敏蛋白,降低IgE结合能力,并在动物模型中缓解过敏反应。针对昆虫蛋白的发酵降敏研究虽相对有限,但由于昆虫与甲壳类过敏原结构相似,因此发酵在调控昆虫蛋白致敏性方面具有良好的前景。
4 未来与展望
昆虫蛋白作为重要的新型替代蛋白来源,其高效、高值开发对构建可持续的全球蛋白质供应体系具有战略意义。然而,致敏性问题是制约其融入主流饮食的关键瓶颈。未来需系统推进“基础研究-工艺创新-产品应用”的全链条突破,围绕过敏原的源头控制,加工过程中的结构调控以及全链条风险治理3个维度协同发力,方能真正释放其营养与经济价值。
在技术创新层面,合成生物学与食品制造技术的融合,为主动调控昆虫蛋白致敏性提供了新路径。一方面,合成生物学工具(如CRISPR/Cas9基因编辑、精准发酵)可用于在分子层面重构蛋白序列,通过敲除主要过敏原基因、修饰IgE表位或引入糖基化位点,从源头创制低致敏原料。另一方面,生物3D打印等先进加工技术,可在产品层面实现过敏原的物理掩蔽,例如将蛋白封装于多糖或脂质基质中,利用空间位阻抑制IgE识别,并调控其在消化道中的释放行为。这种“从分子到产品”的一体化调控策略,不仅有助于降低致敏风险,还能通过质构与风味设计提升产品接受度,为过敏人群提供安全、可定制的蛋白选择。值得强调的是,技术创新必须与全链条风险管控体系的建设同步推进。未来应建立多维度评价体系,整合人工智能预测、体外消化模型、细胞免疫评测及临床数据,构建动态风险评估模型与分级管理数据库。同时,需建立覆盖育种、养殖、加工到消费的全过程追溯系统,完善产品标识与风险沟通机制,实现生产端与消费端的有效联动。
总之,推动昆虫蛋白进入主流膳食,是一项涉及科研、产业与监管的系统工程。唯有通过持续的技术创新与科学的管控体系相结合,才能使其真正成为安全、营养且可持续的蛋白质来源,为全球食物系统转型与人类健康提供坚实支撑。
原文链接:https://kns.cnki.net/kcms2/article/abstract?v=y_SiIdm5mqvu_9m4ZIyDnqk4f5tky1YFyH0bdUPb3m3X5QJMhMaXRHBsSPpbGeMKFnQPI9YDOJJSYQKknShN4ya88uxtJmAj2JpCs0TIXNK8lWOsnHpT3CUOUac2edBkju4xBPGHtbaQmuDOEE0Bc3HF9YqmPCpV5R_U8aYYcFq9YN3APScAEA==&uniplatform=NZKPT&language=CHS


